
24 horas com a química

A química nos acompanha 24 horas por dia. Ela está presente em praticamente todos os produtos que utilizamos no dia a dia. Do sofisticado computador à singela caneta esferográfica, do possante automóvel ao carrinho de brinquedo, não há produto que não utilize matérias-primas fornecidas pela indústria química. Teclados, gabinetes e disquetes dos computadores, para ficar apenas em alguns exemplos, são moldados em resinas plásticas. No automóvel, há uma lista enorme de produtos de origem química: volantes, painéis, forração, bancos, fiação elétrica encapada com isolantes plásticos, mangueiras, tanques de combustível, para-choques e pneus são apenas alguns desses itens.
A maioria dos alimentos chegou às nossas mãos em embalagens desenvolvidas pela química. Em nossas roupas, há fibras sintéticas e corantes de origem química. Em nossa casa, há uma infinidade de produtos fornecidos, direta ou indiretamente, pela indústria química: a tinta que reveste as paredes, potes e brinquedos em plástico, tubos para condução de água e eletricidade, tapetes, carpetes e cortinas. Isso sem falar nos componentes químicos das máquinas de lavar roupas e louças, na geladeira, no micro-ondas, no videogame e no televisor.

Nos produtos que utilizamos em nossa higiene pessoal e na limpeza da casa também podemos perceber a presença da química. é só prestar atenção. Nosso cotidiano seria realmente muito mais difícil sem a química. é para ajudar o homem a ter mais saúde, mais conforto, mais lazer e mais segurança que a indústria química investe dia a dia em tecnologia, em processos seguros e no desenvolvimento de novos produtos. O resultado é o progresso.
De onde vem e para onde vai a química
Já sabemos que a Química nos acompanha a vida toda, a todo o momento. Mas, e de onde vem a Química? Ora, daquilo que também nos acompanha a vida toda, a todo instante: a Natureza. É na natureza que encontramos as matérias-primas, como petróleo, água do mar, que irão compor os produtos os quais, por sua vez, fazem parte de outros produtos. Veja, nos exemplos: Escova de dentes, sabão em pó.
desvendando mistérios com a química
Algumas coisas que nos intrigam quando tomamos ciência delas podem ser facilmente explicadas pela Química. Veja alguns mistérios que selecionamos e encontre as respostas para eles:

Por que o fermento faz o bolo crescer?


As mesmas reações químicas que permitem obter álcool são também as responsáveis pelo crescimento dos pães e bolos.
Mas, primeiro, vamos entender o que é fermentação?
A fermentação é um processo no qual são adicionadas à massa de cereais leveduras que, utilizando açúcares da massa, irão produzir um gás chamado dióxido de carbono (CO2). Este gás fica preso na massa pois ela tem uma estrutura formada pelas proteínas da farinha, o glúten (como se fosse uma rede elástica), fazendo com que a massa cresça. Após assado, esse gás se desprende e a estrutura da massa se mantém rija, porque durante o aquecimento as proteínas da água se ressecam e ficam firmes.
Então, por que o fermento faz a massa crescer?
Porque libera gás carbônico (CO2) em reações químicas, formando bolhas no meio da massa que fazem com que ela aumente de tamanho e fique fofa.Existem dois tipos de substâncias usadas para este fim: o fermento biológico e o fermento químico.
O fermento químico é composto por bicarbonato de sódio (NaHCO3) e um ácido orgânico, que, quando aquecido a uma temperatura de 50 a 60 graus Celcius e em contato com a umidade da massa, reagem e também liberam gás carbônico.
O fermento biológico é composto por microorganismos vivos - leveduras - que se reproduzem graças a temperatura da massa e ao açúcar presente nela, que lhes serve de alimento. Durante a reprodução, os micro-organismos liberam gás carbônico.
Assim...
O conhecido "fermento biológico" nada mais é do que uma grande quantidade de células de Saccharomyces cerevisiae, um grupo de leveduras muito utilizado na fabricação de bebidas alcoólicas, pão, bolos, biscoitos... Este grupo faz parte dos fungos, e engloba organismos unicelulares com nutrição heterotrófica por não possuírem pigmentos fotossintetizantes. De todos os seres vivos, os fungos são os que possuem a mais rica coleção de enzimas. Esta variedade de enzimas permite que eles "ataquem" praticamente qualquer tipo de matéria.
Por que o sabão limpa?
Para pensar nesta resposta, precisamos antes responder outras duas perguntas:
1ª) Para que limpar?
Se for a pele, necessitamos retirar as impurezas que pegamos no dia a dia, equilibrando assim o pH natural, oleosidade e outras características fisiológicas.
Se for a roupa, a retirada da sujeira, deixa-a mais macia, livre de bactérias, melhorando inclusive a transpiração da nossa pele.

2ª) Só a água limpa?
Por que precisamos dela quando usamos o sabão?
A molécula de água é formada por dois átomos de hidrogênio e um de oxigênio.
Bem, se olharmos ao microscópio veremos que os dois átomos de hidrogênio ficam de um lado e o de oxigênio do outro lado.
No hidrogênio temos um único elétron e no oxigênio temos oito, o que acaba criando dois lados distintos: um positivo, próximo do hidrogênio, e um com carga negativa próximo ao oxigênio.
Esta carga positiva que foi criada no lado do hidrogênio termina quando um lado negativo de outra molécula de água é atraída por ele fazendo então com que haja uma ligação temporária entre as moléculas de água deixando-as "unidas".
Esta polaridade também acaba ajudando na limpeza, mas de uma maneira mais fraca, pois não consegue remover certos tipos de sujeira como as gorduras e óleos.
É nesse momento que precisamos do sabão, que vai fortalecer o que era fraco. Se observarmos uma molécula de sabão, veremos uma molécula longa de hidrocarbonetos, como se fosse um fio bem comprido, onde temos uma "cabeça" e um "rabo", duas extremidades que se diferem pela carga como ocorreu com a água!
De uma maneira simples, podemos dizer que a "cabeça" desta molécula adora a água e detesta moléculas de óleo e graxa, já o "rabo" faz o contrário, detesta moléculas de água e adora moléculas de óleo e graxa.

Sendo assim, tendo uma parte apolar que é dada pela gordura e outra parte polar dada pela base, o sabão acaba conseguindo atrair para si moléculas apolares e/ou polares, aumentando o poder de limpeza, envolvendo a sujeira.
CH3 - (CH2)n - CO2 - Na2+
Mas a limpeza não acabou, precisamos tirar o sabão que envolveu a "sujeira" criando pequenos conjuntos que chamamos de MICELAS.
Agora, estas uniões entre moléculas de sabão e gordura acabam ficando dispersas na água impedindo que elas se re-aglomerem pois ficam envolvidas por uma película e acabam se afastando uma das outras pela repulsão das cargas.
Pronto! Agora a sujeira vai embora, sendo levada para o ralo, cano, tubulação... indo para a estação de tratamento de esgotos, é claro!
Como funciona o bafômetro?
No Brasil, temos o costume de dar nomes que tentem popularizar algo, neste caso o "bafômetro" não fugiu à regra!
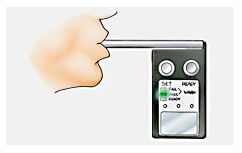
Em inglês, o bafômetro é conhecido como "breath alcohol analyzer" - ANALISADOR DE ÁLCOOL NO HáLITO, ou seja, não é um equipamento para "MEDIR BAFO" e, sim um equipamento que se utiliza de um processo químico tabelado que por comparação acaba calculando a concentração de álcool no sangue de uma pessoa em função do ar que é exalado pelos pulmões.
Mas para entendermos o que acontece devemos saber algumas informações! Em primeiro lugar, o ÁLCOOL analisado é o ETANOL (C2H5OH) que é proveniente de bebidas alcoólicas que são vendidas em bares e outros estabelecimentos comerciais para depois serem ingeridas. Mas de onde vem esta comparação?
Quando uma pessoa ingere álcool, após alguns instantes este álcool acaba indo para a corrente sanguínea em função do nosso processo digestivo sendo absorvido pelo intestino delgado, enviado para a corrente sanguínea para só depois ser metabolizado ("filtrado") pelo fígado. Deste ponto em diante começa o método de análise e, é neste intervalo, antes de ser processado pelo fígado que podemos "ver" e analisar a concentração de álcool no sangue!

Após já existir o etanol na corrente sanguínea, ocorre um equilíbrio químico, onde o ar contido nos pulmões acaba se SATURANDO (excesso) com o etanol presente no sangue, através de outro processo químico chamado de difusão gasosa dos gases, que tem como finalidade transportar os gases metabolizados no nosso corpo.
Agora aparece o "bafômetro"! Este equipamento é muito utilizado hoje em dia para verificar EXCESSOS cometidos por motoristas e até mesmo criminosos em outras situações. Os equipamentos podem ser baseados em medidas de condutividade elétrica usando materiais condutores que são influenciados pelas substâncias químicas do ambiente que se aderem à sua superfície (como óxido de estanho (SnO2), depositados sobre um substrato isolante) ou por medidas espectrofotométricas na região do infravermelho, ou por reações de óxido-redução.
A escolha de um ou mais equipamentos para determinada análise esta apenas dependente da rapidez e/ou necessidade de precisão da análise. Em casos como o de análise imediata, são usados "Bafômetros" portáteis e descartáveis para que exista rapidez e maior capacidade de análise de amostras.
Um método que podemos exemplificar é o de óxido-redução!
Vejamos os passos que devem ser seguidos por um motorista que esta sendo investigado:
1- O motorista deve assoprar com força no canudinho, fazendo com que por arraste conduza o ar de seus pulmões para um analisador contendo uma solução ácida de dicromato de potássio;
2-O álcool presente no "bafo", é convertido em ácido acético conforme mostra a reação abaixo:
3CH3CH2OH + 2K2Cr2O7 + 8H2SO4 --> 3CH3COOH + 2Cr2(SO4)3 + 2K2SO4 + 11H2O
Nesta reação o etanol é convertido a ácido acético e o cromo, na forma de íon dicromato (amarelo alaranjado) é transformado em Cr+3 (coloração verde). Quanto maior a concentração de álcool, mais intensa é a coloração esverdeada obtida.
Segundo a lei n.º 11.705, de 19 de junho de 2008), que alterou diversos dispositivos do Código Brasileiro de Trânsito (lei n.º 9.503/97), o artigo 306 diz que "Conduzir veículo automotor, na via pública, estando com concentração de álcool por litro de sangue igual ou superior a 6 (seis) decigramas, ou sob a influência de qualquer outra substância psicoativa que determine dependência".
No entanto estará passível de multa de R$ 955,00 e suspensão de habilitação, se o resultado estiver acima de 0,1 mg de etanol por litro de ar expelido. E Se for flagrada com uma dosagem superior a 0,3 mg de álcool por litro de ar expelido no bafômetro, o motorista irá responder criminalmente por este ato irresponsável, tendo uma pena que pode variar de seis meses a três anos de prisão.
Por que o refrigerante quente espuma?
Por enquanto ainda estamos em uma época sem muito calor, mas quando chegar o verão...
Quem nunca passou pela situação de pedir na lanchonete um refrigerante ou água gaseificada? E quem após ver a garrafinha aparentemente gelada acaba ficando triste quando aparece o barulho "Shiiiiiiiiiiiiiiiiii...". Logo pensamos: "pronto, está QUENTE!"
Quente? Mas como podemos saber só pelo barulho? Nem chegamos a provar! Vamos compreender então este mistério! Para isso devemos voltar um pouco no tempo e ver como são fabricadas estas bebidas gaseificadas!
A criação do refrigerante se deu aproximadamente no ano de 1676 em Paris, numa pequena empresa que sem saber o que estava fazendo acabou misturando água, sumo de limão e açúcar, para ver no que iria dar... Surgem então décadas de história e milhares de produtos diferentes até chegarmos ao século XX e XXI.
No Brasil, a primeira fábrica começou a produzir em definitivo no ano de 1941, na cidade de Recife/PE. Mas voltemos até a produção!


Inúmeros produtos
Apesar de existirem diferentes sabores, cores e odores, existe um ingrediente que não muda, podendo sim se apresentar em maior ou menor quantidade, mas sempre vai estar lá... o gás carbônico! Sim, ele mesmo! Nós respiramos Oxigênio e liberamos Gás Carbônico para depois no calor ingerirmos novamente! Estranho não é mesmo? Coisas do mundo moderno!
O gás carbônico se encontra dissolvido no refrigerante na forma: CO2 + H2O--> H2CO3--> H+ + HCO3''
Para este processo químico damos um nome específico: carbonatação. Ela ocorre quando o gás carbônico (dióxido de carbono) é adicionado a uma solução aquosa (água) que até o momento no nosso caso chamaremos de XAROPE para só depois da inclusão do Gás que poderemos chamar de refrigerante. O dióxido de carbono reage quimicamente com as moléculas de água formando ácido carbônico.
Esta quantidade de dióxido de carbono dissolvido pode atingir as 8 gramas/litro dependendo do produto que está sendo fabricado.
Só que esse ácido carbônico é muito instável. Ele é gás, e sendo assim quer sair do líquido de qualquer jeito, por isso existe um outro truque! Na fabricação do refrigerante, na hora da sua produção ele está gelado! Faz-se a carbonatação e fecha-se rapidamente (colocando-se tampa ou lacre).
Então o refrigerante é fabricado gelado, compramos quente e gelamos novamente, tudo isso para ingerirmos o Gás Carbônico que havíamos "jogado fora" durante a respiração!
Após o lacre, a pressão dentro da garrafa é maior que a de fora, fazendo com que aquele espaço vazio dentro da garrafa acabe ficando preenchido pelo gás carbônico que está louquinho para sair!
Quando você abre a garrafa, a pressão diminui e o ácido carbônico acaba se transformando de novo em gás carbônico e água. Como o gás demora um pouco para sair, porque existem moléculas de gás carbônico ligadas às moléculas do líquido, quando isso ocorrer, vai ficar tudo sem graça, teremos suco e não refrigerante não é mesmo?
Agora que você já sabe o segredo da espuma e do barulhinho, já pode dizer ao garçom: "Não teria um mais gelado?"
Por que o gesso endurece?
Para responder a essa pergunta, devemos nos lembrar de duas características importantes que envolvem a química!
1º- O endurecimento do Gesso ocorre em função de um processo químico chamado de CRISTALIZAçãO. Este processo ocorre quando a partir de uma solução líquida (mas também podemos ter sólido fundido) se obtém cristais de um dos participantes desta mistura, tendo neste caso uma pureza de 100%.
Em um processo de cristalização, as moléculas se organizam quando se aproximam e vão se agrupando criando estruturas mais rígidas, que chamamos de cristais.
Uma boa experiência de cristalização é criar uma solução supersaturada de água e sal (coloque 5 colheres de sal em um copo de água). Pegue apenas a solução turva e despeje em um recipiente qualquer (tampa de refrigerante por exemplo e/ou pirex) deixe em um lugar sem que a poeira caia sobre ele e aguarde, depois de uns 2 dias a água terá se evaporado e teremos cristais de Cloreto de sódio. Veja ao final o texto uma outra dica!
A segunda informação importante que devemos saber é que o Gesso na verdade é um produto de um processo químico. Neste processo ocorre a desidratação térmica (perda de água) de um mineral chamado de GIPSITA, para só depois ser feita a sua moagem em partículas cada vez menores, até obtermos um pó!

Já que possuímos duas informações básicas, vamos aumentar um pouco mais o nosso conhecimento!
O gesso é um material bem fino (após a moagem), de cor branca quando não está contaminado por impurezas, e que possui a capacidade de após se hidratar e posterior desidratação se cristalizar em formas diversas que o coloca como um produto de grande aceitação comercial, haja visto que sua maleabilidade e capacidade de manter formas diversas agradam tanto visualmente como comercialmente em função do seu baixo custo.
Quimicamente ele é um material vindo de Sulfato de Cálcio e se dá pela mineração e calcinação da Gipsita, que já havia sido formada há cerca de 150 milhões de anos, estando presente em grande parte da superfície do nosso planeta por ter características menos densas.
Mas nem tudo são flores!
O gesso em contato com a água acaba se hidratando novamente, retornando a dihidrato, o que pode causar enfraquecimento da sua estrutura original após a total perda deste excesso de água, o que causará possível troca do material.
Finalizando a experiência: se você desejar ter cristais ainda maiores, coloque algumas gotas daquela mesma solução criada (ou de uma nova) sobre os cristais feitos, um pouquinho por vez e o seu cristal irá crescer cada vez mais. Tente também substituir o sal pelo açúcar e coloque algumas gotas de corante e terás cristais coloridos,OK!
Por que o palito de fósforo pega fogo?
Muita gente pensa que a pólvora está envolvida no processo... NÃO!
Você já ouviu falar em alotropia? Essa é a capacidade de um elemento químico poder formar substâncias simples diferentes. Estes elementos podem ser Oxigênio (O), Enxofre (S), Carbono (C) ou Fósforo (P). E é isso que acontece com o fósforo branco e o fósforo vermelho, ambas formas alotrópicas do fósforo. São sólidos inflamáveis!
O fósforo branco, também chamado de fósforo amarelo, é a forma mais reativa entre todas. Esta forma entra em combustão espontânea no contato com o ar, devendo ser armazenado sob água, na qual é insolúvel. A forma mais estável é o fósforo vermelho. O fósforo vermelho, ao contrario do fósforo branco, não sofre ignição espontânea com o ar.


Na caixinha de fósforo, os ingredientes inflamáveis foram separados: parte na cabeça do palito (clorato de potássio, entre outras), parte do lado de fora da caixa, junto com o material abrasivo. Quando raspamos o palito de fósforo na superfície áspera de sua caixinha, isso faz com que ele acenda, pois este é o fósforo vermelho que rapidamente converte-se em fósforo branco.
Um pouco de história
Os palitos de fósforo começaram a se popularizar em 1826. Apesar de muito grandes em comparação aos atuais (8 cm), o maior inconveniente era o fato de incendiarem-se sozinhos dentro da embalagem. O problema foi solucionado apenas em 1855, quando os ingredientes inflamáveis foram separados em dois, como vimos o início do texto.
Por que os ginastas usam pó nas mãos?
Ao ver a nossa equipe feminina de ginástica olímpica conquistar uma marca histórica, logo pensamos que foi preciso muita garra para não deixar escorregar das mãos a oportunidade de apresentar a evolução do Brasil neste esporte.
E não deixaram escorregar mesmo! Não apenas em função da técnica, mas também com a ajuda do Pó de Magnésio!
Sim, isso mesmo! Sem o uso daquele pó branco que passam nas mãos não só as brasileiras, mas todas as outras ginastas poderiam ESCORREGAR!


Mas o que acontece?
Começou o exercício, então é necessário mais energia, a respiração aumenta para se obter uma maior quantidade de oxigênio que irá gerar mais energia, com isso, tudo começa a mudar.
Durante o exercício físico, a temperatura do corpo aumenta devido ao gasto maior de energia por parte do organismo, em conseqüência disso, temos um aumento da temperatura e acabamos transpirando mais, pois o suor é uma tentativa do corpo de diminuir a temperatura...ele está se PROTEGENDO!
Com o aparecimento do SUOR, acaba ocorrendo um menor atrito com as superfícies no caso as traves etc. O atrito ocorre quando duas superfícies entram em contato, superfícies lisas acabam escorregando entre si, já superfícies mais rugosas acabam tendo mais resistência durante o movimento entre elas.
Daí o problema, não podemos parar de SUAR, mas podemos tentar minimizar o problema que ele causa (o suor)! Para isso usamos o Pó de Magnésio!
Na verdade este é Pó tem o nome químico de CARBONATO DE MAGNéSIO (MgCO3), que é um sal de origem natural no mineral conhecido como MAGNESITA.
A sua ação química se dá neste caso na sua capacidade de ANTIUMECTAR, ou seja, ele possui a capacidade de evitar absorção da umidade fazendo com que se torne uma BARREIRA SECA ENTRE A MãO SUADA E A SUPERFíCIE no caso das ginastas. Com isso haverá mais atrito sem os riscos de queda e escorregamento.
Como curiosidade em função da sua não toxidade, alguns antiumectantes como o próprio Carbonato de Magnésio são utilizados em alimentos para que estes não absorvam a umidade do meio ambiente. é o caso do macarrão, vá até a sua cozinha e veja se na embalagem contém a descrição: ANTIUMECTANTES e seus símbolos são:
Carbonato de cálcio=AU.I Carbonato de magnésio=AU.II
Pronto, você agora sabe que o pó de magnésio, se estiver em condições próprias, é usado até na nossa comida!
Você tem mais algum mistério desse tipo?



